- May -akda Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:52.
- Huling binago 2025-06-01 07:38.
Mahalagang Pagkakaiba - Methane vs Ethane
Methane at Ethane ang pinakamaliit na miyembro ng pamilyang alkane. Ang mga molecular formula ng dalawang organic compound na ito ay CH4 at C2H6 ayon sa pagkakabanggit. Ang pangunahing pagkakaiba sa pagitan ng Methane at Ethane ay ang kanilang kemikal na istraktura; ang isang molekula ng Ethane ay maaaring ituring bilang dalawang pangkat ng methyl na pinagsama bilang isang dimer ng mga pangkat ng methyl. Ang iba pang mga kemikal at pisikal na pagkakaiba ay pangunahing lumitaw dahil sa pagkakaiba sa istruktura na ito.
Ano ang Methane?
Ang
Methane ay ang pinakamaliit na miyembro ng alkane family na may chemical formula CH4 (apat na hydrogen atoms ang naka-bonding sa isang carbon atom). Ito ay itinuturing na pangunahing bahagi ng natural gas. Ang methane ay isang walang kulay, walang amoy at walang lasa na gas; kilala rin bilang carbane, marsh gas, natural gas, carbon tetrahydride, at hydrogen carbide. Madali itong maapoy, at ang singaw nito ay mas magaan kaysa sa hangin.
Ang
Methane ay natural na matatagpuan sa ilalim ng lupa at sa ilalim ng sahig ng dagat. Ang atmospheric methane ay itinuturing na isang greenhouse gas. Nasira ang methane sa CH3- na may tubig sa atmospera.
Ano ang Ethane?
Ang
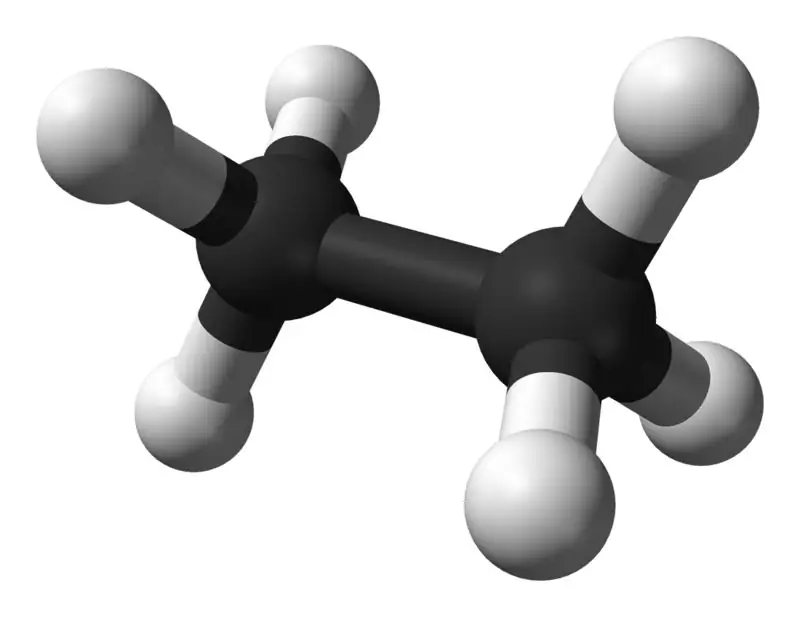
Ethane ay isang walang kulay, walang amoy na gaseous compound sa karaniwang temperatura at presyon. Ang molecular formula at molecular weight nito ay C2H6 at 30.07 g·mol−1 ayon sa pagkakabanggit. Ito ay nakahiwalay sa natural na gas, bilang isang byproduct mula sa proseso ng pagdadalisay ng petrolyo. Napakahalaga ng ethane sa paggawa ng ethylene.
Ano ang pagkakaiba ng Methane at Ethane?
Mga Katangian ng Methane at Ethane
Istruktura:
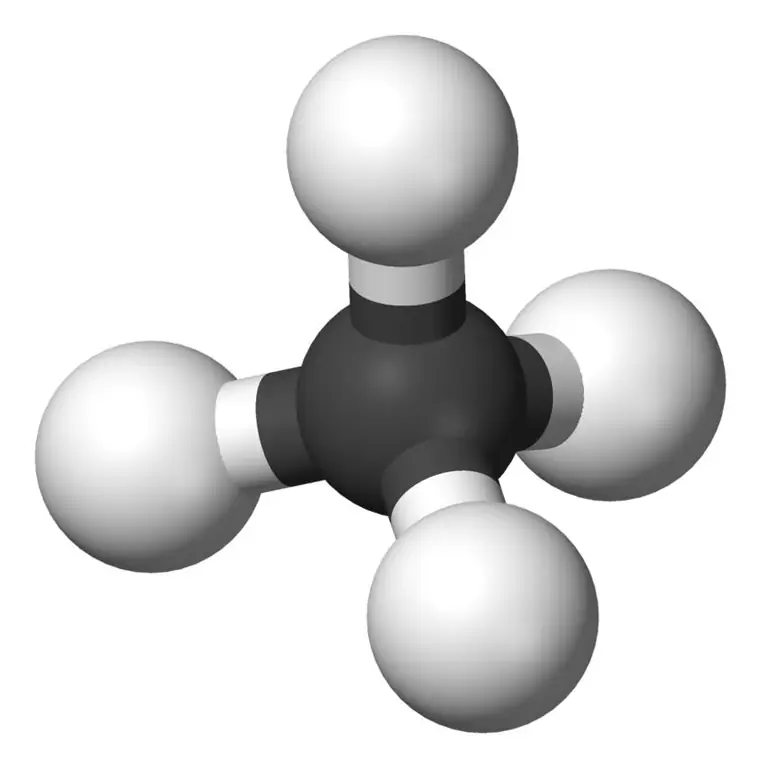
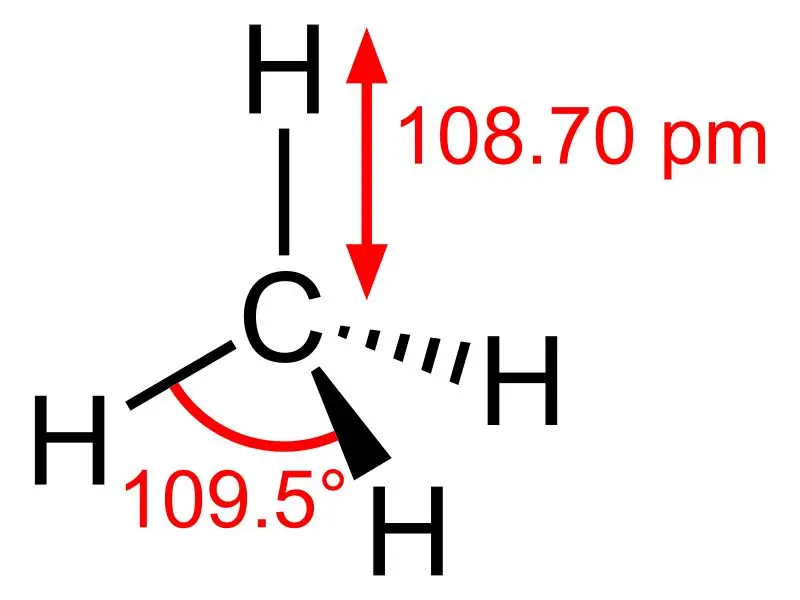
Methane: Ang molecular formula ng methane ay CH4, at ito ay isang halimbawa ng isang tetrahedral molecule na may apat na katumbas na C-H bond (sigma bonds). Ang anggulo ng bond sa pagitan ng H-C-H atoms ay 109.50 at lahat ng C-H bond ay katumbas, at ito ay katumbas ng108.70 pm.
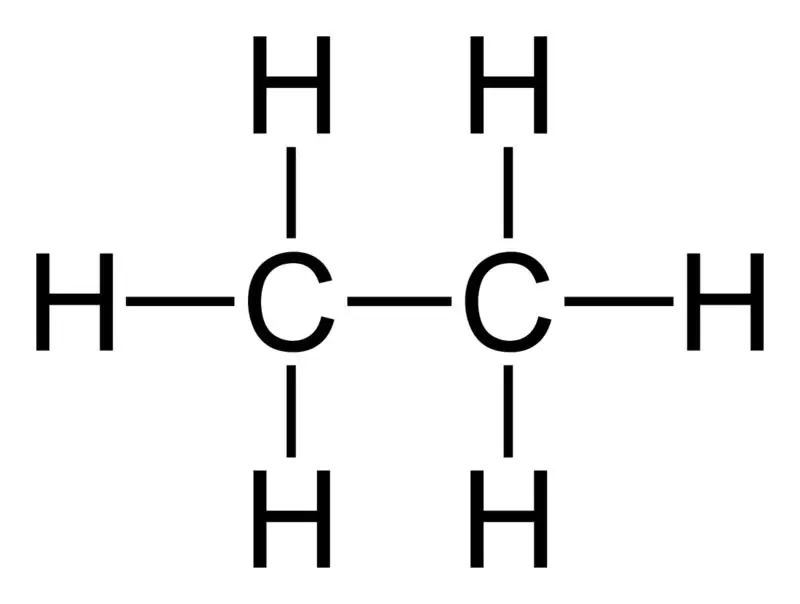
Ethane: Ang molecular formula ng ethane ay C2H6,at ito ay isang saturated hydrocarbon dahil hindi ito naglalaman ng maraming bond.
Mga Katangiang Kimikal:
Methane:
Stability: Ang methane ay isang chemically very stable na molekula na hindi tumutugon sa KMnO4, K2Cr 2O7, H2SO4 o HNO 3 sa ilalim ng normal na mga kondisyon.
Pagsunog: Sa pagkakaroon ng sobrang hangin o oxygen, nasusunog ang methane na may maputlang asul na apoy na gumagawa ng carbon dioxide at tubig. Ito ay isang mataas na exothermic na reaksyon; samakatuwid, ito ay ginagamit bilang isang mahusay na gasolina. Sa pagkakaroon ng hindi sapat na hangin o oxygen, bahagyang nasusunog ito sa carbon monoxide (CO) gas.
Mga Reaksyon ng Pagpapalit: Ang methane ay nagpapakita ng mga reaksyon ng pagpapalit na may mga halogens. Sa mga reaksyong ito, ang isa o higit pang hydrogen atoms ay pinapalitan ng pantay na bilang ng halogen atoms at ito ay tinatawag na “halogenation.” Ito ay tumutugon sa chlorine (Cl) at bromine (Br) sa pagkakaroon ng sikat ng araw.
Reaksyon sa Steam: Kapag ang pinaghalong methane at steam ay dumaan sa isang pinainit na (1000 K) nickel na sinusuportahan sa ibabaw ng alumina, maaari itong makagawa ng hydrogen.
Pyrolysis: Kapag pinainit ang methane sa humigit-kumulang 1300 K, nabubulok ito sa carbon black at hydrogen.
Ethane:
Mga Reaksyon: Ang ethane gas (CH3CH3) ay tumutugon sa bromine vapor sa pagkakaroon ng liwanag upang bumuo ng bromoethane, (CH 3CH2Br) at hydrogen bromide (HBr). Ito ay isang reaksyon ng pagpapalit; isang hydrogen atom sa ethane ay pinapalitan ng bromine atom.
CH3CH3 + Br2 à CH3 CH2Br + HBr
Combustion: Ang kumpletong combustion ng ethane ay gumagawa ng 1559.7 kJ/mol (51.9 kJ/g) ng init, carbon dioxide, at tubig.
2 C2H6 + 7 O2 → 4 CO 2 + 6 H2O + 3120 kJ
Maaari rin itong mangyari nang walang labis na oxygen, na gumagawa ng pinaghalong amorphous carbon at carbon monoxide.
2 C2H6 + 3 O2 → 4 C + 6 H 2O + enerhiya
2 C2H6 + 5 O2 → 4 CO + 6 H 2O + enerhiya
2 C2H6 + 4 O2 → 2 C + 2 CO + 6 H2O + enerhiya atbp.
Mga Depinisyon:
Mga reaksyon ng pagpapalit: Ang reaksyon ng pagpapalit ay isang kemikal na reaksyon na kinasasangkutan ng paglilipat ng isang functional group sa isang kemikal na compound at pinalitan ito ng isa pang functional group.
Mga Paggamit:
Methane: Ginagamit ang methane sa maraming pang-industriyang proseso ng kemikal (bilang gasolina, natural gas, liquefied natural gas) at dinadala ito bilang isang refrigerated fluid.
Ethane: Ang Ethane ay ginagamit bilang panggatong para sa mga motor at bilang nagpapalamig para sa isang napakababang sistema ng temperatura. Ito ay ipinadala sa mga silindro ng bakal bilang isang liquefied gas sa ilalim ng sarili nitong vapor pressure.






